Hướng dẫn đọc bài 43: Pha chế dung dịch, SGK Hóa học 8. Bài 1 Nội dung 2 3 4 5 Trang 149 SGK Hóa Học 8 bao gồm Toàn bộ Lý thuyết, Công thức lập phương trình hóa học, Phương trình hóa học, Chuyên đề Hóa học… Giúp học sinh học tốt môn Hóa học lớp 8.
Lý thuyết
1. Cách pha chế dung dịch theo nồng độ cho trước
– Trước hết ta xác định chất nào là chất tan, chất nào là dung môi.
– Có hai hỗn hợp:
+ Pha chế dung dịch theo nồng độ phần trăm
+ Pha chế dung dịch dựa vào nồng độ mol.
2. Cách pha loãng dung dịch đến một nồng độ nhất định
Dưới đây là lời giải Bài 8 trang 149 SGK hóa học 1 2 3 4 5. Các em đọc kỹ tên bài trước khi giải nhé!
Bài tập
giaibaisgk.com sẽ giới thiệu đến các bạn đầy đủ phương pháp trả lời, giải bài tập môn Hóa 8 có lời giải và đáp án chi tiết SGK Hóa 8 trang 2 3 4 5 Bài 1 để các bạn tham khảo. Chi tiết lời giải, đáp án từng bài tập các em tham khảo dưới đây:
1. Trả lời 1 Trang 149 SGK Hóa học 8
Làm bay hơi 60 gam nước từ dung dịch 15% thu được dung dịch 18% mới. Xác định khối lượng của dung dịch ban đầu.
Giải pháp thay thế:
Cho khối lượng ban đầu của dung dịch là mg
Vậy khối lượng dung dịch sau khi bay hơi là: (m – 60) gam
Khối lượng chất tan có trong dung dịch trước và sau khi bay hơi không đổi, ta có:
mct = \(\frac{15.m}{100}\) = \(\frac{18(m-60)}{100}\)
Xem Thêm: Thước lỗ ban cửa đi, thông số vàng để đón sinh khí cho ngôi nhà
⇔ 15. mét = 18(mét – 60)
⇔ 15m = 18m – 1080
⇔ 3m = 1080
⇔m=360g
Vậy khối lượng ban đầu của dung dịch là 360 gam.
2. Trả lời câu 2 SGK Hóa học 8 trang 149
20 g dung dịch cuso4 được đun nóng nhẹ cho đến khi nước bay hơi thu được cuso4 khan ở dạng chất rắn màu trắng. Khối lượng của chất là 3,6 g. Xác định nồng độ phần trăm của dung dịch cuso4
Giải pháp thay thế:
Xem Thêm: Cách đo khoảng cách trên Google Maps chính xác giữa các điểm
Phần trăm giải pháp:
c% = \(\frac{m_{ct}}{m_{dd}}\) . 100% = \(\frac{3,6}{20}\) . 100% = 18%
3. Giải bài 3 SGK Hóa học 8 trang 149
Cân 10,6 g na2co3 cho vào cốc chia độ 500 ml. Đổ từ từ nước cất vào cốc cho đến khi đạt vạch 200 mL. Khuấy nhẹ cho đến khi tan hết na2co3 ta được dung dịch na2co3. Chúng ta biết rằng 1 mL dung dịch này có khối lượng 1,05 gam. Xác định nồng độ phần trăm (c%) và nồng độ mol của dung dịch vừa pha chế.
Giải pháp thay thế:
Rất nhiều dung dịch na2co3:
mét = 200. 1,05 = 210 gam
Xem Thêm: Cách đo khoảng cách trên Google Maps chính xác giữa các điểm
Phần trăm giải pháp:
c% = \(\frac{10.6}{210}\) . 100% = 5,05%
Số mol của na2co3 là:
n = \(\frac{10.6}{(46+12+48)}\) = 0,1 mol
Nồng độ mol của dung dịch:
cm = \(\frac{0.1.1000}{200}\) = 0,5 m
4. Giải bài 4* trang 149 SGK Hóa học 8
Điền các ô trống trong bảng bằng các giá trị chưa biết bằng cách thực hiện các phép tính trên từng cột:

Giải pháp thay thế:
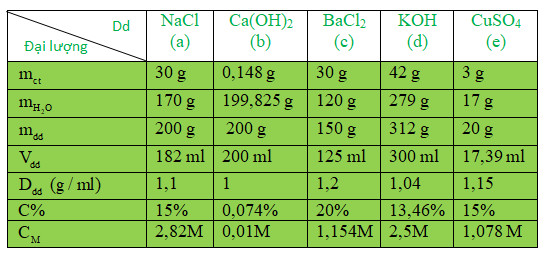
5. Giải bài 5* trang 149 SGK Hóa học 8
Qua phương pháp thí nghiệm người ta đo độ tan của muối trong nước và thu được kết quả như sau:
– Nhiệt độ của dung dịch diệt muỗi bão hòa là 200C.
– Khối lượng của chén sứ là 60,26 g.
Xem Thêm: BẬT MÍ NHỮNG Ý NGHĨA THÚ VỊ CỦA HÌNH XĂM KIM CƯƠNG
– Khối lượng cốc sứ đựng dung dịch muối là 86,26 g.
– Khối lượng của chén nung và muối kết tinh sau khi bay hơi là 66,26 g.
Xác định độ tan của muối ở 200c?
Giải pháp thay thế:
Ta có: mdd = 86,26 – 60,26 = 26 (gam)
mct = 66,26 – 60,26 = 6 (gam)
Ở 20°C, hòa tan 6 gam muối trong 20 gam nước để tạo thành dung dịch bão hòa. Vậy ở 20°C, 100g nước sẽ hòa tan rất nhiều muối:
\(s = {{100 \times 6} \over {20}} = 30\left( {gam} \right)\)
Vậy độ tan của muối ở 20°C là 30g.
Câu trước:
- Hướng dẫn giải 1 2 3 4 5 6 7 Trang 145 146 SGK Hóa học 8
- Hướng dẫn giải 1 2 3 4 5 6 Trang 151 SGK Hóa học 8
- Giải các bài toán hóa học lớp 8 khác
- Học tốt môn toán lớp 8
- Học tốt vật lý lớp 8
- Học tốt môn sinh học lớp 8
- Học tốt ngữ văn lớp 8
- Điểm tốt môn lịch sử lớp 8
- Học tốt môn địa lý lớp 8
- Học tốt tiếng Anh lớp 8
- Học tốt môn tiếng Anh lớp 8 thí điểm
- Học Tin học lớp 8
- Học chăm chỉ môn gdcd lớp 8
Câu tiếp theo:
Xem thêm:
Trên đây là hướng dẫn Giải trang 1 2 3 4 5 trang 149 SGK Hóa học 8 đầy đủ và ngắn gọn nhất. Chúc các bạn ôn thi môn hóa lớp 8 thật tốt!
“Môn thể thao nào đã khó giabaisgk.com”


