I. Vị trí nguyên tử và cách sắp xếp electron

– Photpho ở chu kỳ 3, ô 15 của bảng tuần hoàn các nguyên tố hóa học.
– Cấu hình electron: 1s22s22p63s23p3
⇒ Lớp ngoài cùng có 5 electron nên hợp chất photpho có thể có hóa trị 5.
Ngoài ra, trong một số hợp chất, photpho có hóa trị 3.
Hai. Tính chất vật lý
Photpho có thể tồn tại ở nhiều dạng thù hình khác nhau, quan trọng nhất là p trắng và p đỏ.
1. Phốt pho trắng
-Sáp không màu hoặc vàng nhạt.

Vết sưng 1: Phốt pho trắng
– Phân tử p4 có cấu trúc tinh thể đặc.
Hình 2: mô hình phân tử p4
– Photpho trắng mềm, dễ nóng chảy (tnc = 44,1ºc).
– Rất độc và gây bỏng nặng nếu rơi vào da.
Xem thêm: 2 cách khắc phục lỗi thiếu, ẩn thanh công cụ trong adobe photoshop
Xem Thêm: Cây cau Lụa
– Không tan trong nước nhưng tan trong các dung môi hữu cơ: c6h6, cs2,…
– Bốc cháy trong không khí ở nhiệt độ trên 40°c.
⇒ Ngâm nước để bảo quản.
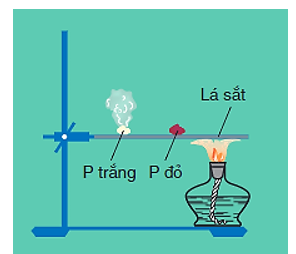
Đạn 3: Thí nghiệm chứng minh khả năng bắt lửa khác nhau của p trắng và p đỏ
– Ở nhiệt độ phòng, photpho trắng phát huỳnh quang màu xanh lục trong bóng tối.
Lưu ý: Phốt pho trắng chuyển dần thành phốt pho đỏ (dạng ổn định hơn) khi đun nóng đến 250°c trong điều kiện không có không khí.
2. phốt pho đỏ
– Phốt pho đỏ là chất bột màu đỏ nóng chảy, hút ẩm.

Bump 4: Phốt pho đỏ
– Photpho đỏ bền trong không khí ở nhiệt độ phòng và không phát huỳnh quang trong bóng tối.
-Không tan trong các dung môi thông thường.
– Chỉ bốc cháy ở nhiệt độ trên 250°c.
– Khi nung nóng trong điều kiện không có không khí, photpho đỏ biến thành hơi nước, khi làm lạnh hơi nước ngưng tụ thành photpho trắng.
– Photpho đỏ có cấu trúc cao phân tử nên khó nóng chảy và khó bay hơi hơn photpho trắng.
Đọc thêm: Viết thư nhân Ngày Thế giới phòng chống AIDS, ngày 1 tháng 12 năm 2003 Viết Tập 12 1 Tuần 6 (trang 80)
Xem Thêm: GIÁC CHÚNG SANH HỮU TÌNH – NGỘ NHẬP PHẬT TRI KIẾN
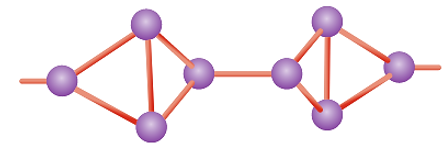
Tập 5: Cấu trúc polyme của phốt pho đỏ
Hai. Tính chất hóa học
– Độ âm điện p < n nhưng p hoạt động hóa học mạnh hơn n2 do liên kết n ≡ n bền hơn.
– P trắng hoạt động hóa học mạnh hơn p đỏ.
– Các mức số oxi hóa của p là: -3, 0, +3, +5.
⇒ p là chất khử hay chất oxi hóa khi nó tham gia phản ứng hóa học.
1. Sự oxy hóa
– Phản ứng với một số kim loại để tạo thành photphua kim loại.
Ví dụ:
2p0+3ca→to⟩ca3p−32 Kansi
2. khả năng loại trừ
– Phản ứng với các phi kim phản ứng như oxy, halogen, lưu huỳnh và các chất oxy hóa mạnh khác.
+ phản ứng với oxy
Thiếu oxy: 4p + 3o2→đến 2p2o3
Thừa oxy: 4p + 5o2 → đến 2p2o5
Xem thêm: Chúng ta còn bao lâu nữa mới hết quân dịch vào năm 2023?
Xem Thêm: Top ghi bàn europa league nhiều nhất Cúp C2
+ Tác dụng với Clo
+ Phản ứng với hợp chất: p dễ phản ứng với các hợp chất có tính oxi hóa mạnh, như hno3 đặc, kclo3, kno3, k2cr2o7,…
6p + 5kclo3 → đến 3p2o5 + 5kcl
Ba. trạng thái tự nhiên
-p có hoạt tính hóa học cao nên không thể tìm thấy dạng tự do trong tự nhiên.
– Hầu hết p đều ở dạng photphat. Hai khoáng vật phốt pho chính là apatit 3ca3(po4)2.caf2 và đá phốt phát ca3(po4)2.

Mảnh thứ sáu: một số khoáng chất phốt pho
Bốn. Ứng dụng và điều chế
1. Ứng dụng
– Sản xuất axit photphoric, sản xuất diêm.

Hình 7: Hộp diêm
– Cũng được sử dụng cho mục đích quân sự: sản xuất bom, cocktail Molotov, bom khói…
2. điều chế
– Về mặt công nghiệp, phốt pho đỏ được sản xuất bằng cách nung hỗn hợp đá phốt phát (hoặc apatit), cát và than cốc đến khoảng 1200ºc trong lò điện.
– Hơi photpho thoát ra khi làm lạnh ngưng tụ lại tạo thành photpho trắng rắn.


